(2: 中国科学院南京地理与湖泊研究所湖泊与环境国家重点实验室,南京 210008)
(3: 中国科学院大学,北京 100049)
(2: State Key Laboratory of Lake Science and Environment, Nanjing Institute of Geography and Limnology, Chinese Academy of Sciences, Nanjing 210008, P.R.China)
(3: University of Chinese Academy of Sciences, Beijing 100049, P.R.China)
湖泛是近二十年来常见于我国浅水湖泊的一种极端水环境问题[1-4],在我国太湖、巢湖等重要湖泊中均曾有发现.2007年,由于湖泛造成自来水变色发臭,导致无锡市居民饮用水安全受到严重威胁,也使得湖泛问题成为政府、学界及公众关注的焦点[2, 5].
湖泛发生时水体通常呈现的共同特征有[6-8]:极低的溶解氧(DO)浓度(接近于0 mg/L)、极低的氧化还原电位(Eh)、较低的pH值、高营养盐负荷以及水体发黑发臭等.对于水体发黑的主要原因,研究者[9-10]认为金属硫化物(主要为铁硫化物,如FeS等)在上覆水体中的累积导致水体颜色逐渐变深并最终发黑.湖泛发生前通常会经历DO和Eh的迅速降低,在这一过程中,Fe2+和ΣH2S在沉积物-水界面处迅速累积并形成FeS等致黑物质[6],因此湖泛发生过程中水体通常自下而上逐渐变黑,这一过程短则数小时,长则数天.水体变黑通常是判断湖泛发生的主要标志,而水体发臭难以去除可能对饮用水安全造成更大的威胁.
已有对野外水体湖泛发生过程中致臭物质的研究表明,无论是藻源性[2]还是草源性[7]湖泛,主要致臭物质可能为嗅味物质,包括土腥素(Geosmin)、二甲基异莰醇(MIB)和2-甲氧基-3-异丁基吡嗪(IBMP等),及挥发性硫化物(volatile sulfur compounds,VSCs),包括硫化氢(H2S)、二甲基硫醚(dimethyl sulfide,DMS)、二甲基二硫醚(dimethyl disulfide,DMDS)、二甲基三硫醚(dimethyl trisulfide,DMTS)和甲硫醇(methanethiol,MTL)等,其中尤以MTL、DMS、DMDS和DMTS等挥发性有机硫化物(VOSCs)为主.然而,这些致臭物质的主要来源及其产生机制至今仍无较为详尽的报道.前期研究[11]已表明,有机质对水体发黑具有重要诱导作用,然而,只有含硫有机物才具有致臭作用,且含硫氨基酸为湖泛发生过程中VOSCs的主要前驱物质.由于许多水生生物体内都含有一定量的含硫氨基酸,而湖泛发生时VOSCs的前驱物含硫氨基酸是否来源于这些水生生物,又是通过怎样的途径进行转化,至今尚未见报道.因此,本文在野外湖泛监测采样的基础上,研究了不同水生生物诱导下湖泛的发生情况,并以蛋氨酸为前驱物质,通过设置不同的降解体系探讨含硫氨基酸代谢产生VOSCs的可能途径,以期进一步揭示生源性湖泛发生过程中水体主要致臭物的产生机制.
1 材料与方法 1.1 野外湖泛监测与采样本研究3个调查采样点(1# 31°23′11″N,120°17′44″E;2# 31°26′6″N,120°22′37″E;3# 31°21′12″N,120°14′29″E)均分布在太湖贡湖湾内,是2007年太湖发生水危机事件的区域.除监测主要致臭物质外,同时还分别监测3个点位的水体基本理化性质和营养盐浓度.分别于2010年5 9月每月中旬(该段时间通常为太湖蓝藻聚集密度较高的季节)在3个采样点采集500ml水样,采集水样时确保水流益出瓶口,迅速用螺口螺紧.同时采集500ml水样用于测定总磷(TP)、总氮(TN)、铵态氮(NH4+-N)、磷酸盐(PO43--P)和叶绿素a(Chl.a)浓度.现场应用水质速测仪(YSI)测定水体的pH、氧化还原电位(Eh)以及溶解氧(DO).所采集样品放入冷藏保温箱内保存,于4 h内带回实验室进行分析.
1.2 模拟实验采样点及样品采集采样点选择在太湖月亮湾水域(31°24′35.8″N,120°6′4.6″E),其水域面积为10.51 km2,位于太湖北部梅梁湾与竺山湾间,是太湖典型的蓝藻堆积区域和湖泛易发区域.使用柱状采样器(φ90mm × 500mm)在该区域采集无扰动柱状样品,同时采集上覆水用于室内模拟实验.
1.3 实验设计 1.3.1 生源性湖泛模拟由于生物残体中含有大量含硫氨基酸,因此,为了验证生源性湖泛发生过程中致臭物质的产生与生物残体的关系,在室内使用Y型沉积物再悬浮发生装置[12]模拟多种生物堆积下湖泛的发生情况.主要实验组有:未添加生物残体的对照组、添加5000g/m2太湖鲜藻组、添加1000g/m2大型浮游动物残体组(主要是枝角类和桡足类,使用13#浮游生物网,以“8”字型从水体中捞取)、添加5000g/m2底栖动物残体组(将去壳后的河蚬残体剪碎加入)、添加5000g/m2鱼类残体组(将太湖梅鲚鱼残体捣碎后加入)以及添加5000g/m2水生植物残体组(将太湖菹草剪碎后加入).温度设置为28℃,水深为1.8 m,接近太湖平均水深[13].观察湖泛是否发生并检测湖泛发生时水体中致臭物质浓度.
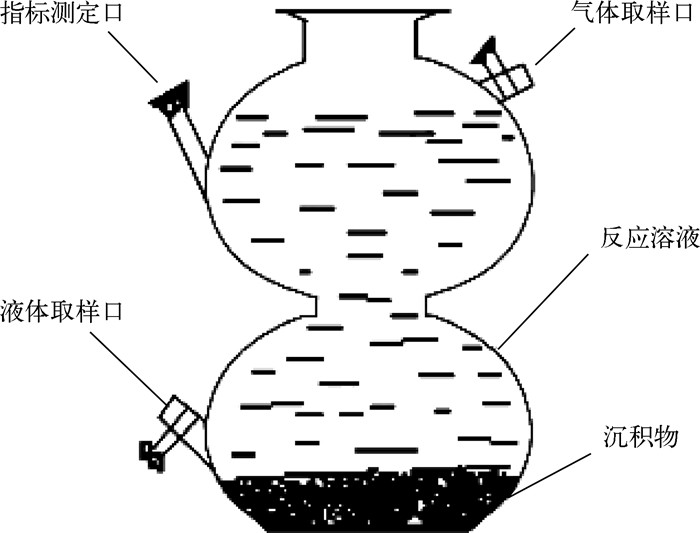
1.3.2 非生物因素对蛋氨酸降解生成致臭物的影响将表层0~6cm原位沉积物充分混匀后称取600g放入具有气密性的密闭反应系统中(图 1)[11],将原位采集的湖水过滤去除悬浮颗粒物之后配制成1.0g/L的蛋氨酸溶液,于121℃下灭菌40min后加入上述反应系统中.共设置3个处理:好氧(DO> 6 mg/L)光照、厌氧(DO < 0 mg/L)光照和厌氧避光,定时取水样测定VOSCs浓度,以研究氧气与光照等非生物因素对含硫氨基酸降解生成VOSCs的影响.
|
图 1 密闭反应系统示意图 Fig.1 Schematic diagram of the airtight reaction system |
向反应系统中加入不同溶液设置5个实验组:对照,高温高压灭菌(121℃灭菌60min),添加2.0mmol/L钨酸钠作为硫酸盐还原菌(SRB)抑制剂,添加5.0mmol/L溴乙基磺酸钠(BES)作为产甲烷菌抑制剂,添加50ml SRB118菌液[14].
通过研究含硫氨基酸降解过程中NH4+-N以及α-酮丁酸、α-羟丁酸、4-甲硫基-2-氧代丁酸(KMBA)等中间产物的生成情况,研究含硫氨基酸的降解过程.
1.4 样品分析野外采集水样中致臭物的测定采用顶空-固相微萃取(HS-SPME)-GC-MS(Agilent1790-5975C)系统组合完成.测试方法及条件详见文献[15];水体中的TN和TP浓度均采用过硫酸钾氧化-比色法测定;NH4+-N和PO43--P浓度均采用Skalar流动分析仪测定;Chl.a浓度采用丙酮提取-分光光度法分析.
蛋氨酸采用亚硝基铁氰化钾-可见分光光度法测定[16];水样中挥发性硫化物分析由顶空固相微萃取(HS-SPME)预浓缩系统和Agilent 7890A/5973N GC-MS(安捷伦公司,美国)系统组合完成;气体样品的分析使用气相色谱-火焰光度检测器Agilent 7890A GC-FPD完成,测试方法及条件详见文献[11].
蛋氨酸代谢中间产物采用Agilent 1200 HPLC测定,仪器配置及方法如下:检测器为二极管阵列检测器(DAD),色谱柱采用Agilent Eclipse XDB-C18 (固定相液膜厚度5 μm,内径4.6mm×长度150mm),配自动进样器.以0.02mol/L的KH2PO4缓冲盐水溶液(A相)和乙腈为流动相(B相),采用梯度洗脱的方式由初始比例A : B为95 : 5经15min洗脱至A : B为80 : 20,恒定流速为1ml/min,检测波长为215 nm,柱温为30℃,进样量为20 μl.
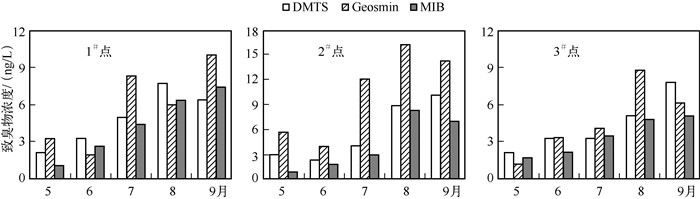
2 结果与讨论 2.1 湖泛易发水域主要致臭物及水体基本理化参数从野外采集的实际样品看,太湖贡湖湾3个采样点水体中的Geosmin、MIB和DMTS是主要致臭物质,其分布具有一定的季节变化规律,在蓝藻暴发初期其浓度处于一个相对较低的水平,而在蓝藻暴发中后期部分蓝藻处于衰亡阶段时,其浓度则相对较高(图 2).
|
图 2 太湖贡湖湾3个采样点主要致臭物浓度的季节变化 Fig.2 Seasonal changes of the main odorous substances concentrations of the three sampling sites in Gonghu Bay of Lake Taihu |
从各监测点位检测到的致臭物浓度变化范围来看,与Yang等[2]在2007年的测定值有较大偏差,其在贡湖湾水体中测得的主要致臭物为DMTS,浓度最高可达11399 ng/L,而在本研究中Geosmin、MIB和DMTS均为野外样品主要致臭物质,其中DMTS浓度最大只有10.1 ng/L,如此大的偏差反映出两者之间的形成机制存在显著差别. Yang等[2]推断在2007年水危机中的高浓度DMTS是由未知的大型污水团造成的,不排除外来污染的因素.而本研究中的DMTS则有可能只是蓝藻暴发后在局部小区域造成厌氧,从而引起局部小区域蓝藻逆境生长甚至死亡.由于蓝藻细胞自身含有大量的Geosmin和MIB,在蓝藻暴发死亡的初期,藻细胞在极度厌氧条件下死亡破裂后其胞内嗅味物质会大量进入水溶液,造成溶解性嗅味物质浓度升高[17];随着藻体进一步降解,其中所含的含硫氨基酸发生分解产生挥发性硫化物,但由于小分子的挥发性硫化物(如H2S、MTL、DMS和DMDS)的饱和蒸汽压较大,挥发性比较强,野外采样难以捕捉到,因此只有挥发性低的DMTS检出.由于太湖是一个大型开放水体,因此小区域内各种化学或生物过程同时并存,各阶段的产物也因此混合在一起.
各监测点位水体基本理化性质和主要营养盐参数的季节变化见表 1.监测区域中的TP、TN以及其它水体参数(如pH、Eh、DO以及Chl.a等)与往年太湖水体中的浓度[3-4]并无太多差异,维持在一个正常的水平.
| 表 1 太湖贡湖湾水体基本理化性质和营养盐浓度变化 Tab.1 The changes of basic physical-chemical properties and nutrient concentrations of water in Gonghu Bay of Lake Taihu |
监测区水体的TP、NH4+-N以及Chl.a与水体中的主要致臭物质呈显著或极显著关系(表 2),说明这些因素可能是影响水体中致臭物质浓度分布的主要因素,在蓝藻暴发、死亡期间,蓝藻不但释放出代谢物质(如土腥素和二甲基异莰醇)和一些营养盐(如NH4+-N),同时还会增加水体的悬浮颗类物浓度,导致水体TP和Chl.a浓度增加.有关这些致臭物质的产生机理需要进一步研究.
| 表 2 太湖贡湖湾水体主要异味物质与基本理化参数的相关性 Tab.2 The correlation between basic physical-chemical parameters and main odor substances of water in Gonghu Bay of Lake Taihu |
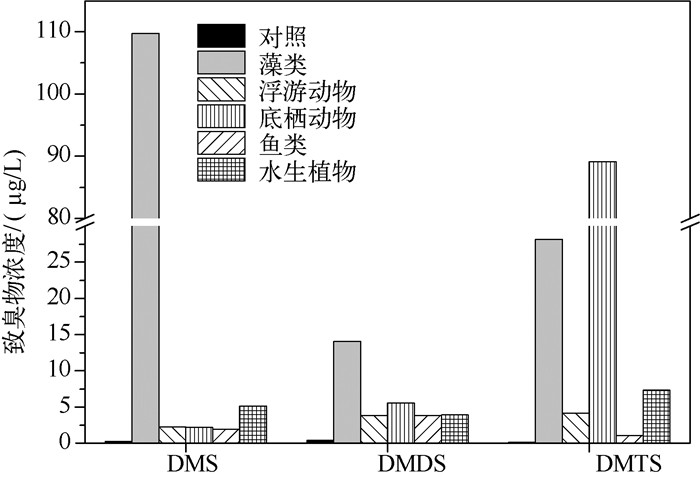
前期研究[11]已表明,有机质对水体发黑具有重要诱导作用,然而,只有含硫有机物才具有致臭作用,且含硫氨基酸为湖泛发生过程中VOSCs的主要前驱物质.由于许多水生生物体内都含有一定量的含硫氨基酸,而湖泛发生时VOSCs的前驱物含硫氨基酸是否来源于这些水生生物,又是通过怎样的途径转化,至今尚未见报道.本研究发现,添加不同生物残体后,水体均发生不同程度的湖泛.各实验组水体中均检出DMS、DMDS和DMTS等主要湖泛致臭物质,且均超出各物质的嗅阈值(DMS、DMDS和DMTS的嗅阈值分别为2.5、0.1和10 ng/L)[18].可见,生源性湖泛发生过程中VOSCs的产生与水生生物有着重要关联.添加藻类时产生的VOSCs浓度相对高于其他实验组(图 3).其原因一方面是藻类代谢过程中会产生VOSCs[19-20],另一方面是太湖蓝藻中含硫氨基酸浓度较高[21],因而藻类死亡降解过程中也会产生大量的VOSCs.虽然底栖动物及水生植物残体产生的一些硫化物浓度也较高,但与蓝藻相比,这些生物在湖泊水体中大量聚集并死亡的概率极小,因此可以推断藻源性湖泛是太湖最为常见的一种湖泛,藻体中大量的含硫氨基酸导致湖泛发生时水体VOSCs浓度激增[2].
|
图 3 不同生源湖泛发生时水体致臭物浓度 Fig.3 Concentrations of odorous compounds during the black blooms induced by various organisms |
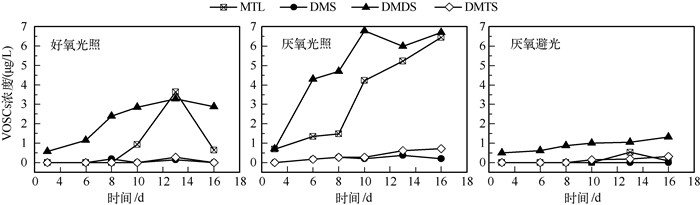
在生源性湖泛发生过程中,氧气、光照等非生物因素均可能对含硫氨基酸降解为VOSCs的过程产生影响.不同氧气及光照条件下蛋氨酸降解生成VOSCs,其浓度随时间变化情况(图 4)表明,厌氧及光照均能促进蛋氨酸非生物降解生成VOSCs,其中DMDS与MTL为非生物降解产生的主要VOSCs组分,也有少量DMTS和DMS产生,但并未检测到H2S.同为光照条件下,厌氧分解产生的DMDS和MTL为好氧分解的2~3倍,而同为厌氧条件下,光照产生的DMDS和MTL最高浓度分别为6.78和6.44 μg/L,比避光条件下DMDS(1.32μg/L)和MTL(0.53μg/L)浓度高5~10倍左右.可见,在蛋氨酸非生物降解过程中,光降解是非常重要的一个因素,厌氧也是促使蛋氨酸降解转化为VOSCs的重要原因之一,但光照条件的影响大于氧气条件的影响.
|
图 4 氧气及光照条件对蛋氨酸非生物降解生成VOSCs的影响 Fig.4 The production of VOSCs from methionine degradation influenced by oxygen and illumination conditions |
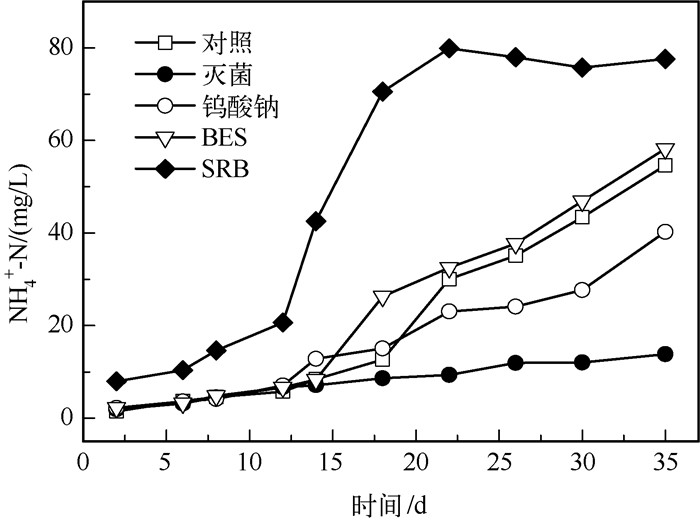
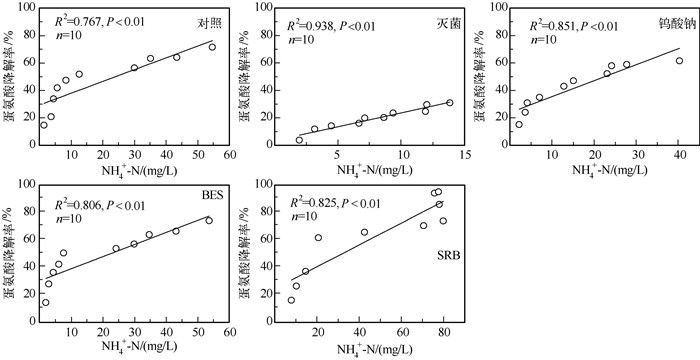
从不同蛋氨酸降解体系中NH4+-N浓度的变化情况来看(图 5),添加SRB菌液的处理NH4+-N浓度最高,其后依次为添加BES(甲烷菌抑制剂)处理、对照处理、添加钨酸钠(SRB抑制剂)处理和灭菌处理.对各处理组NH4+-N浓度与相应的蛋氨酸降解率进行相关性分析后发现(图 6),各处理组蛋氨酸降解率均与NH4+-N浓度呈极显著相关(P < 0.01),表明生物或非生物作用下,蛋氨酸降解的第一步会发生脱氨基作用或脱甲硫基作用形成NH4+-N、α-羟丁酸、α-酮丁酸和4-甲硫基-2-氧代丁酸等.而从各组NH4+-N浓度变化来看,添加SRB菌液的处理组NH4+-N浓度与其他实验组间呈极显著相关(P < 0.01),说明SRB在含硫氨基酸降解过程中有着重要的作用,这也与前期研究所发现的SRB对湖泛的重要作用相符[14].
|
图 5 不同蛋氨酸降解体系中NH4+-N浓度变化 Fig.5 Variations of NH4+-N concentrations under different methionine degradation treatments |
|
图 6 不同处理组中NH4+-N浓度与蛋氨酸降解率的相关关系 Fig.6 Correlations between NH4+-N concentration and methionine degradation rate under different treatments |
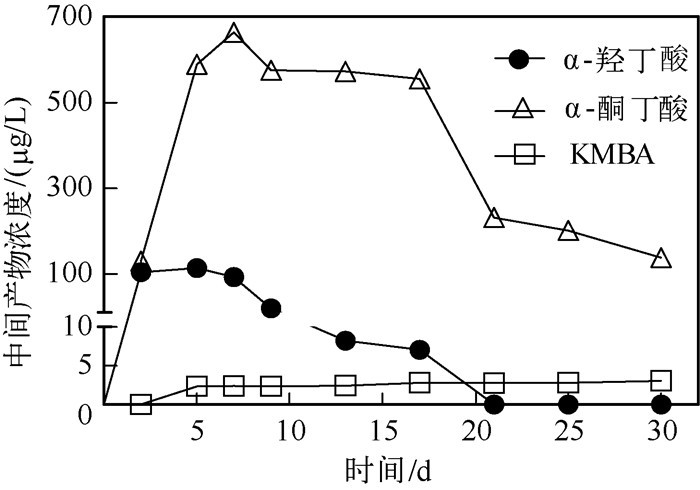
为探讨蛋氨酸降解的途径,除对NH4+-N和VOSCs等进行监测外,还需对含硫氨基酸降解过程中产生的α-羟丁酸、α-酮丁酸和KMBA等中间产物动态变化进行研究.α-酮丁酸在实验开始后浓度即迅速升高,并于7 d内达到最高值,之后随着进一步降解而逐渐降低.与α-酮丁酸相似,α-羟丁酸在实验进行5 d后浓度达到最高,随后浓度迅速降低并最终完全消失,但其浓度要比α-酮丁酸低得多(图 7).而KMBA的浓度则始终保持在较低水平(0~3.1 mg/L),其原因一方面可能是由于KMBA会快速发生脱甲硫基作用转化为MTL,造成体系中KMBA无法大量累积;另一方面可能是蛋氨酸除发生脱氨基作用生成KMBA外,还可同时发生脱氨基作用和脱甲硫基作用,直接一步生成MTL、α-酮丁酸和氨,由此导致体系中KMBA浓度较低而α-羟丁酸和α-酮丁酸却有较明显的累积过程.
|
图 7 蛋氨酸降解主要中间产物浓度变化 Fig.7 Dynamics of three intermediates concentration during the metabolism of methionine |
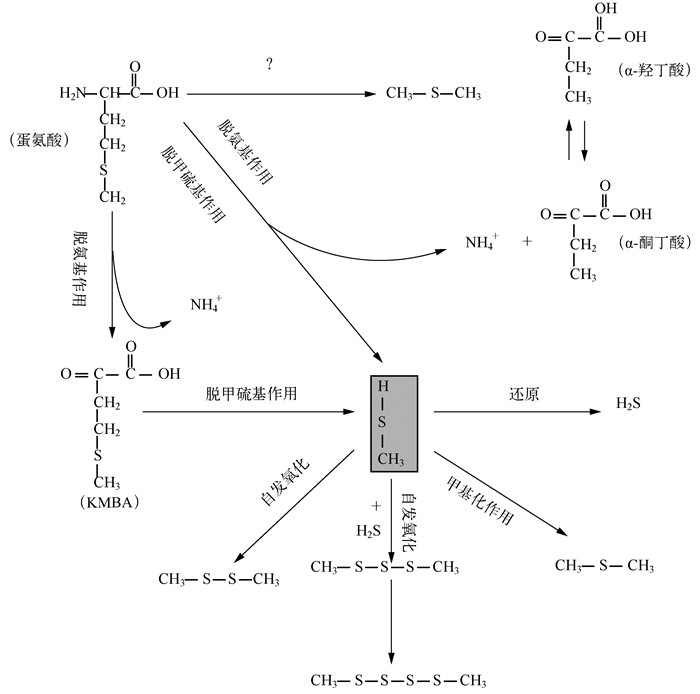
根据本文的研究结果以及前期的一些研究[11, 22],推测蛋氨酸降解生成VOSCs的可能途径如图 8所示.
|
图 8 蛋氨酸降解为VOSCs的可能途径 Fig.8 Proposed pathways of the catabolism of methionine to VOSCs |
在室内模拟条件下对生源性湖泛发生过程中水体含硫致臭物产生情况以及含硫氨基酸转化为VOSCs的机制进行研究,主要结论如下:
1) 各类水生生物残体均能诱导湖泛的发生,其中,藻源性湖泛发生时水体中VOSCs浓度升高尤为突出,藻类代谢以及藻体中含有的大量含硫氨基酸可能是这一现象发生的主要原因.
2) 在含硫氨基酸降解产生VOSCs的过程中,光照和厌氧条件能有效促进降解的进行,其中光照的作用尤为突出.
3) 无论是在生物还是非生物体系中,蛋氨酸降解率与NH4+-N浓度均存在显著相关性(P < 0.01),表明蛋氨酸降解的第一步反应应是脱氨基作用.
4) KMBA在含硫氨基酸降解体系中难以累积,而α-羟丁酸和α-酮丁酸则有较明显的累积过程,表明脱氨基作用发生后可能很快即会发生脱甲硫基作用,且二者有可能同时发生,由这两种反应生成MTL,随后再生成DMS、DMDS、DMTS和H2S等.
| [1] |
陆桂华, 马倩. 2009年太湖水域"湖泛"监测与分析. 湖泊科学, 2010, 22(4): 481-487. |
| [2] |
Yang M, Yu J, Li Z et al. Taihu Lake not to blame for Wuxi's woes. Science, 2008, 319: 158-158. |
| [3] |
申秋实, 周麒麟, 邵世光等. 太湖草源性"湖泛"水域沉积物营养盐释放估算. 湖泊科学, 2014, 26(2): 177-184. DOI:10.18307/2014.0202 |
| [4] |
刘国锋, 何俊, 范成新等. 藻源性黑水团环境效应:对水沉积物界面处Fe、Mn、S循环影响. 环境科学, 2010, 31(11): 2652-2660. |
| [5] |
Zhang XJ, Chen C, Ding JQ et al. The 2007 water crisis in Wuxi, China:Analysis of the origin. Journal of Hazardous Materials, 2010, 182(1/2/3): 130-135. |
| [6] |
Shen Q, Liu C, Zhou Q et al. Effects of physical and chemical characteristics of surface sediments in the formation of shallow lake algae-induced black bloom. Journal of Environmental Sciences, 2013, 25(12): 2353-2360. DOI:10.1016/S1001-0742(12)60325-8 |
| [7] |
Shen Q, Zhou Q, Shang J et al. Beyond hypoxia:Occurrence and characteristics of black blooms due to the decomposition of the submerged plant Potamogeton crispus in a shallow lake. Journal of Environmental Sciences, 2014, 26(2): 281-288. DOI:10.1016/S1001-0742(13)60452-0 |
| [8] |
申秋实, 邵世光, 王兆德等. 风浪条件下太湖藻源性"湖泛"的消退及其水体恢复进程. 科学通报, 2012, 57(12): 1060-1066. |
| [9] |
Stahl JB. Black water and two peculiar types of stratification in an organically loaded strip-mine lake. Water Research, 1979, 13(5): 467-471. DOI:10.1016/0043-1354(79)90040-X |
| [10] |
Duval B, Ludlam SD. The black water chemocline of meromictic Lower Mystic Lake, Massachusetts, USA. International Review of Hydrobiology, 2001, 86(2): 165-181. DOI:10.1002/(ISSN)1522-2632 |
| [11] |
卢信, 冯紫艳, 商景阁等. 不同有机基质诱发的水体黑臭及主要致臭物(VOSCs)产生机制研究. 环境科学, 2012, 33(9): 3152-3159. |
| [12] |
范成新. 一种室内模拟水下沉积物再悬浮状态的方法及装置: 中国, 200410014329, 2005.
|
| [13] |
Qin B, Xu P, Wu Q et al. Environmental issues of lake Taihu, China. Hydrobiologia, 2007, 581(1): 3-14. DOI:10.1007/s10750-006-0521-5 |
| [14] |
Feng Z, Fan C, Huang W et al. Microorganisms and typical organic matter responsible for lacustrine "black bloom". Science of the Total Environment, 2014, 470: 1-8. |
| [15] |
李学艳, 陈忠林, 沈吉敏等. 固相萃取-气质联机测定水中嗅味物质2-甲基异茨醇和土霉素. 中国环境监测, 2006, 22(2): 18-21. |
| [16] |
邵晨, 黎雷, 于水利等. 产嗅藻类对东太湖某地原水中嗅味物质2-MIB的贡献. 中国环境科学, 2014, 34(9): 2328-2333. |
| [17] |
McCarthy TE, Sullivan M. A new and highly specific colorimetric test for methionine. Journal of Biological Chemistry, 1941, 141(3): 871-876. |
| [18] |
Watson SB. Aquatic taste and odor:A primary signal of drinking-water integrity. Journal of Toxicology and Environmental Health-Part a-Current Issues, 2004, 67(20/21/22): 1779-1795. |
| [19] |
Ginzburg B, Chalifa I, Gun J et al. DMS formation by dimethylsulfoniopropionate route in freshwater. Environmental Science and Technology, 1998, 32(14): 2130-2136. DOI:10.1021/es9709076 |
| [20] |
Hu HY, Mylon SE, Benoit G. Volatile organic sulfur compounds in a stratified lake. Chemosphere, 2007, 67(5): 911-919. DOI:10.1016/j.chemosphere.2006.11.012 |
| [21] |
李克朗. 太湖蓝藻资源化利用可行性研究[学位论文]. 无锡: 江南大学, 2009.
|
| [22] |
Lu X, Fan CX, He W et al. Sulfur-containing amino acid methionine as the precursor of volatile organic sulfur compounds in algea-induced black bloom. Journal of Environmental Sciences, 2013, 25(1): 33-43. DOI:10.1016/S1001-0742(12)60019-9 |
 2015, Vol. 27
2015, Vol. 27 

