枝角类是淡水水体浮游动物的一个重要类群,不同种类间个体大小差别非常大,其群落结构特征与食物链能量传递效率密切相关[1].大型滤食性种类,尤其是溞(Daphnia),生长快,滤食能力强,在与小型枝角类种类的食物竞争中,具有强的竞争性优势[2].但是,溞与小型枝角类种类间的食物竞争受捕食、食物质量和组成等因素调节[3-4].溞虽然对小型枝角类种类有竞争优势,但对鱼类的捕食敏感.浮游生物食性鱼类对大个体种类的选择性捕食抑制了溞对小型枝角类种类的竞争强度,造成浮游动物群落结构小型化,降低了浮游动物对浮游植物的牧食压力,从而导致水体呈现更高的叶绿素与总磷比值[5-6].
食物质量是调节枝角类种间竞争强度的另一个重要因素.磷是细胞中DNA、RNA、细胞膜和ATP等的组成元素之一,约占动物干重的1 %左右[7].其中,约49 % ~63 %的磷用于合成核酸[7].由于核糖体RNA与蛋白质合成有关,核糖体RNA的含量决定了蛋白质的合成速率,从而决定了生物的生长速度[8].通常情况下,大型滤食性枝角类——溞的RNA含量高于小型枝角类种类,相应地,它们体内磷含量以及生长速率高于小型枝角类种类[9-10].但是,高的体内磷含量意味着它们对食物磷含量要求比较高.在食物(碳)充足的情况下,溞的生长对食物中碳磷比值有一定的要求.一般而言,在食物碳磷比为100~300(碳磷比阈值)时,溞的生长不受磷限制.当食物碳磷比超过300时,它们的生长受磷限制,体内磷以及RNA含量下降,生长减缓[11-13];而当食物碳磷比低于120时, 溞的个体生长率同样下降,呼吸速率上升, 增加应对食物碳磷不平衡的代谢投入[14].此外,浮游动物也会在生理上以及行为上作出一些积极的调整以应对食物磷限制,尽量减少食物磷限制对生长的影响,如:提高对食物中磷的同化效率、增加摄食率、选择性牧食低碳磷比食物等[15-16].
中国南亚热带地区水体属磷限制水体,浮游植物通常呈现高碳磷比的特征,浮游动物生长易受磷限制.浮游植物磷限制对浮游动物生长的影响既有直接的也有间接的[17].直接影响是浮游植物的低磷可获得性产生的化学计量学影响;间接影响是非化学计量学的,是由于磷缺乏可能导致浮游植物细胞变大、细胞壁增厚以及不饱和脂肪酸含量降低等,从而对浮游动物的个体生长和生殖产生影响[18-20].盔型溞(D. galeata)和脆弱象鼻溞(Bosmina fatalis)分别是该地区水体大型枝角类和小型枝角类的代表种类.脆弱象鼻溞在水体中全年均有分布;盔型溞只出现在鱼类捕食压力相对比较低的季节(枯水期末期至丰水期早期),而在高鱼类捕食压力季节,盔型溞一般从水层中消失[21].在温带湖泊中,溞属通常在鱼类捕食压力比较低的春末夏初与其他浮游动物的食物竞争中取得优势,并导致湖泊在该时期出现一个清水期[22].基于个体大小和体内磷含量,盔型溞在低鱼类捕食压力季节与小型枝角类的食物竞争中应该可以取得优势.但是,在中国南亚热带水体中,虽然盔型溞在低鱼类捕食压力季节可以与小型枝角类同时出现在水体中,但盔型溞并不占优势,种群密度远低于小型枝角类种类,如:脆弱象鼻溞[21].食物磷限制是否削弱了盔型溞对脆弱象鼻溞的竞争优势?针对上述问题,我们比较分析了盔型溞和脆弱象鼻溞在3种碳磷比食物条件下的种群增长情况,探讨食物碳磷比对它们竞争的调节作用.
1 材料与方法 1.1 实验动物与食物的培养盔型溞和脆弱象鼻溞均采自广州流溪河水库.在实验室,每个种类均只挑选出一个雌性个体,喂以2 mg C/L的蛋白核小球藻(Chlorella pyrenoidosa)(碳磷比为105)进行单克隆培养.培养用水为用孔径为0.22 μm的滤膜过滤的流溪河水库水(磷浓度处于检测限以下).培养条件为:温度25℃,光周期L :D = 14 h :10 h.在实验开始的前一天,将即将孵化出幼体的母体移入到新鲜的过滤水库水中,获取龄长小于24 h的幼溞用于实验.
实验用蛋白核小球藻用BG-11培养基培养(25℃,光周期L :D=14 h :10 h).在培养不同碳磷比蛋白核小球藻前,取蛋白核小球藻母液以3000转/min的速度离心10 min,去掉上清液,加无氮、无磷的BG-11培养基再次离心去掉上清液,随后加入到无氮、无磷的BG-11培养基中,饥饿培养2 d.为获取低碳磷比、中碳磷比和高碳磷比蛋白核小球,基于BG-11培养基配方,将培养基中磷的浓度分别调整为230、23和5.75 μmol/L,培养蛋白核小球藻(25℃,光周期L :D = 14 h :10 h).在对数生长期,将蛋白核小球藻液以3000转/min的速度离心10 min,去掉上清液,加无菌蒸馏水再次离心去掉上清液,随后加入到适量的无氮、无磷的BG-11培养基中,避光4℃保存.同时,取适量小球藻液过滤到已称重的孔径为0.22 μm的滤膜上,在60℃下烘24 h,称重.小球藻碳含量用元素分析仪(vario EL cube,德国)测定;磷含量采用钼酸铵分光光度法测定,测定前先用碱性过硫酸钾将样品消解. 3种培养条件下获取的蛋白核小球藻碳磷比分别为105、740和2400.
1.2 实验处理实验设计高磷、中磷和低磷3个食物质量处理组,碳磷比分别为105、740和2400;3个动物处理组:盔型溞单独培养、脆弱象鼻溞单独培养以及盔型溞和脆弱象鼻溞混合培养.蛋白核小球藻浓度为2 mg C/L,超过盔型溞和脆弱象鼻溞的食物阈浓度,并且每天更换培养液, 确保实验过程中动物生长不受碳限制,实验动物种群能够进行指数增长至少3周以上.每个处理组设3个重复,每个实验组中枝角类初始密度为33 ind./L(300 ml过滤流溪河水库水,10只枝角类).对于混和培养处理组,盔型溞和脆弱象鼻溞按密度比例1 :1接种到培养液中,盔型溞和脆弱象鼻溞之间并不隔离.培养条件为温度25℃,光照强度1200 lx,光周期L :D = 14 h :10 h.每天将枝角类转移至新配制的具有2 mg C/L小球藻的过滤水库水中,并计数.实验持续时间为26~42 d,在种群密度达到最大密度后出现快速下降趋势时终止实验.实验结束时,在解剖镜下测量体长,每个平行每个种类随机测量30个个体.
1.3 数据处理与分析种群增长率的计算参照Sibly等的方法[23].将每个平行的种群密度取对数,然后与实验时间进行回归分析,回归方程的斜率即为种群增长率.为了分析食物质量对种间竞争强度的影响,用1-
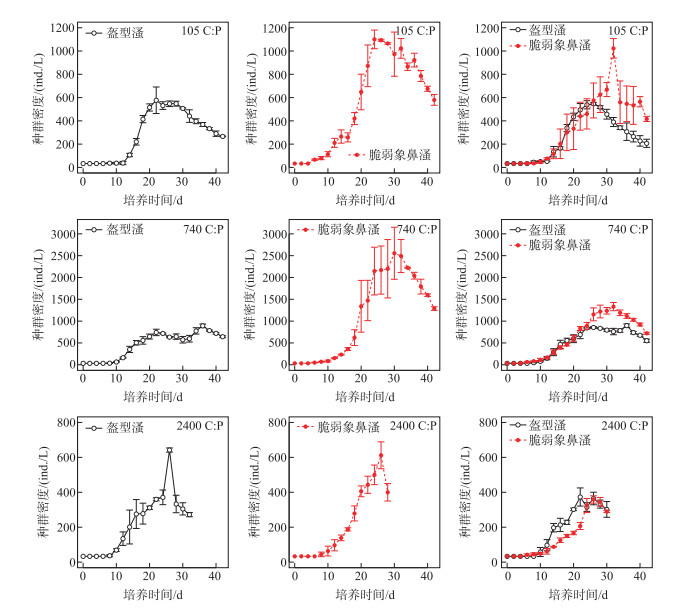
盔型溞和脆弱象鼻溞不管是单独培养或混合培养,不管食物质量条件如何,在培养的前10 d,种群生长均处于一个平缓期,然后进入指数增长期,并在26 d后种群密度达到最大值(图 1).盔型溞和脆弱象鼻溞平均最大种群密度分别为378~893和364~2399 ind./L;平均种群增长率分别为0.11~0.14和0.09~0.16 d-1(图 2);平均体长分别为1.53~2.50和0.25~0.35 mm(图 3).双因素方差分析表明,食物质量对盔型溞的种群增长率和最大种群密度均有显著性影响;脆弱象鼻溞的种间竞争对盔型溞的种群增长率没有显著性影响,但对盔型溞的最大种群密度有显著影响,并与食物质量存在显著的交互作用(表 1).食物质量和盔型溞的种间竞争对脆弱象鼻溞的种群增长率和最大种群密度均有显著性影响,而且均存在显著性的交互作用(表 1).
|
图 1 在3种碳磷比食物条件下盔型溞和脆弱象鼻溞单独培养或混合培养时的种群增长曲线(均值±标准差) Fig.1 Population growth curves of D. galeata and B. fatalis cultured alone or together (competition) on food with three different C:P ratios (Shown are the mean ± standard deviation based on 3 replicates) |
|
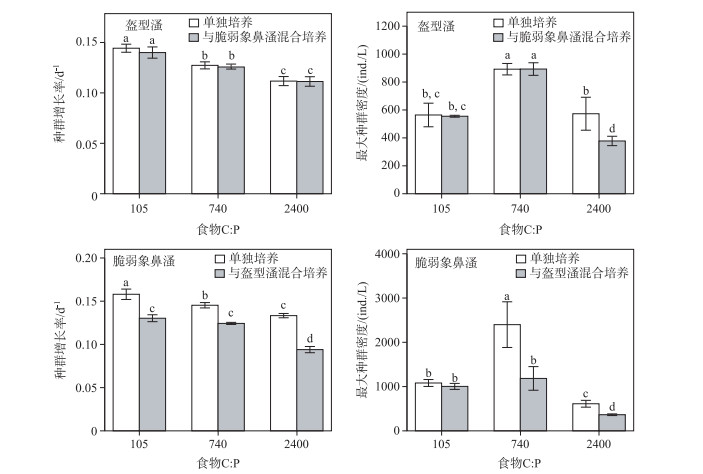
图 2 盔型溞和脆弱象鼻溞在单独培养或混合培养时的种群增长率和最大种群密度 (均值±标准差,标准差线上有相同的字母表示没有显著性差异(P > 0.05, Tukey多重比较)) Fig.2 Rate of population increase and peak population densities of D. galeata and B. fatalis cultured separately or together on food of different qualities (Shown are the mean ± standard deviation based on 3 replicates. For each treatment, data bars carrying similar letter designations (a, b, c and d) are not statistically significant (P > 0.05, Tukey test)) |
|
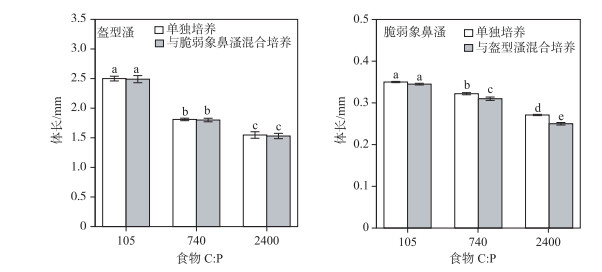
图 3 在3种碳磷比食物条件下脆弱象鼻溞和盔型溞单独培养或混合培养时的体长 (均值±标准差,标准差线上有相同的字母表示没有显著性差异(P > 0.05, Tukey多重比较)) Fig.3 Body length of B. fatalis and D. galeata cultured separately or together on food of different qualities (Shown are the mean ± standard deviation based on 3 replicates. Left panel: D. galeata, Right panel: B. fatalis. For each treatment, data bars carrying similar letter designations (a, b, c, d and e) are not statistically significant (P > 0.05, Tukey test)) |
| 表 1 食物质量和种类竞争对两种枝角类种群增长率和最大种群密度影响的双因素方差分析 Tab. 1 Results of two-way analysis of variance performed on the peak population densities and rates of population increase of D. galeata and B. fatalis cultured separately or together on food of different qualities |
多重比较分析结果表明,在相同的动物处理组中,盔型溞和脆弱象鼻溞的种群增长率和种群平均体长均随着食物碳磷比的升高而显著下降;而它们的最大种群密度在食物碳磷比为740的处理组显著高于另外两个食物碳磷比处理组(图 2和3).在相同食物质量条件下,盔型溞的种群增长率在单独培养和与脆弱象鼻溞混合培养间无显著差异;脆弱象鼻溞的种群增长率在与盔型溞混合培养时显著低于单独培养时(图 2).在食物碳磷比为105和740处理组,盔型溞的最大种群密度在单独培养和与脆弱象鼻溞混和培养间无显著差异;在食物碳磷比为2400处理组,盔型溞的最大种群密度在与脆弱象鼻溞混合培养时显著低于单独培养时(图 2).在食物碳磷比为105处理组,脆弱象鼻溞的最大种群密度在单独培养和与盔型溞混合培养间无显著差异;在食物碳磷比为740和2400处理组,脆弱象鼻溞的最大种群密度在与盔型溞混合培养时显著低于单独培养时(图 2).在相同食物质量条件下,两个种类的平均体长在单独培养和混合培养间均无显著差异(图 3).
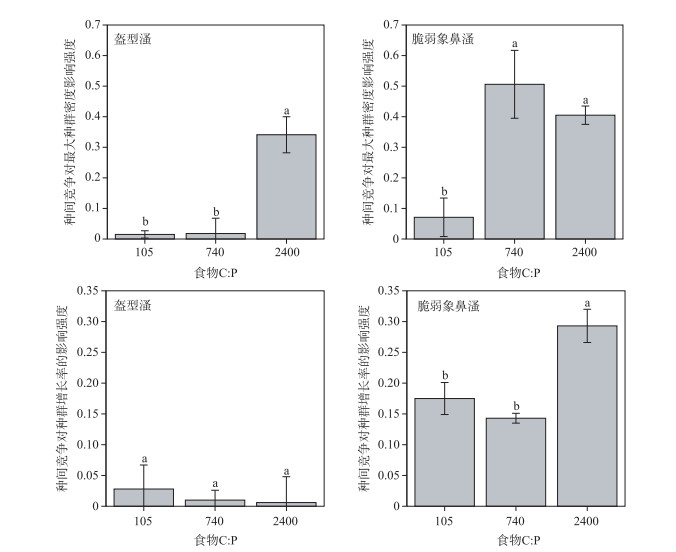
脆弱象鼻溞的种间竞争对盔型溞最大种群密度的影响程度在食物碳磷比为105和740处理组几乎可以忽略不计,但在食物碳磷比为2400处理组的平均影响程度为0.34.脆弱象鼻溞的种间竞争在3个食物质量处理组中均对盔型溞的种群增长率无显著影响.盔型溞的种间竞争对脆弱象鼻溞的最大种群密度影响程度在食物碳磷比为105的处理组几乎可以忽略不计,但在食物碳磷比为740和2400处理组平均影响程度分别为0.51和0.41.盔型溞的种间竞争对脆弱象鼻溞的种群增长率平均影响程度为0.14~0.29,而且在在食物碳磷比为2400处理组显著高于其他两个处理组(图 4).
|
图 4 在3种碳磷比食物条件下种间竞争对最大种群密度和种群增长率的影响 (均值±标准差,标准差线上有相同的字母表示没有显著性差异(P > 0.05, Tukey多重比较)) Fig.4 The magnitude of the competition effect on the peak population density and the population growth rate of competing species on food of different qualities (For each treatment, data bars carrying similar letter designations (a and b) are not statistically significant (P > 0.05, Tukey test)) |
盔型溞属大型滤食性枝角类,体内含磷量高、个体生长率快、寿命长、净生殖率高,但幼体期比较长[24-25].相反,脆弱象鼻溞则属小型枝角类,体内含磷量低、个体生长率较慢、寿命短、净生殖率低,但幼体期比较短[24].溞属各种类凭借高的个体生长率、高的净生殖率和强的滤食能力在与小型枝角类种类的食物竞争中取得优势[26].小型枝角类种类虽然个体生长率相对较低、寿命短、净生殖率低,但通过缩短幼体期,尽早进入成龄期的方式来维持高的种群增长率,增强种群的食物竞争强度[24].虽然溞个体生长快、生殖率高,但对食物磷含量要求比较高,生长比较容易受磷限制.当食物碳磷比分别超过300时,溞的个体生长率下降、首次产仔时间延长、产仔量降低,从而导致内禀增长率下降[11, 13].象鼻溞对磷的需求量低于溞,在食物碳磷比高于600时生长才会受到磷限制[27-28].本研究有两个食物处理组碳磷比超过600,因此,在这两个处理组中,盔型溞和脆弱象鼻溞的生长受磷限制,种群增长率和体长均显著小于碳磷比为105的处理组.但是,在碳磷比为740的处理组,两种枝角类的最大种群密度均显著高于碳磷比为105的处理组.这种情形的出现可能与两种枝角类在面对食物磷限制时所采取的生活史策略调整有一定的关系.在食物磷不受限制时,由于种间竞争强度低,不需要通过提高种群密度来获取竞争优势.它们可以尽量产生更大的卵,同时体内具有更高的磷含量,让个体生长率维持在较高水平上,导致体型大型化,但单位磷承载的最大种群密度反而比较低.相反,在食物磷限制情形下,它们下调体内磷含量,牺牲个体生长率,个体小型化,但能将磷更多的投入到生殖中,提高单位磷承载的最大种群密度,以维持种群的食物竞争强度.
根据“大小效率假说”,大型枝角类对小型枝角类具有竞争优势.但是,在自然水体中,枝角类不仅要面对食物竞争,同时还要面对浮游生物食性鱼类的捕食和食物质量不佳等问题.浮游生物食性鱼类的选择性捕食、食物磷限制或不饱和脂肪酸缺乏等因素可以削弱大型枝角类的竞争优势,让小型枝角类取替大型枝角类成为优势种类[2, 29-31].如:在温带湖泊,大型枝角类通常在春末夏初是优势浮游动物种类,给浮游植物施予强的牧食压力,导致湖泊出现一个清水期,但之后随着鱼类捕食压力的增强以及蓝藻成为优势浮游植物类群,浮游动物群落结构小型化[22]. Iwabuchi和Urabe比较分析了具有相同体内磷含量的大型滤食性枝角类蚤状溞(D. pulex)和小型枝角类方形网纹溞(Ceriodaphnia quadrangula)的竞争能力,发现在以浮游植物为唯一食物来源的情况下,不管食物是否磷限制,蚤状溞对方形网纹溞均有竞争优势,但在食物包括浮游植物和细菌两种来源时,方形网纹溞反而比蚤状溞有竞争优势[32].他们认为蚤状溞只能从浮游植物获取磷,而方形网溞除了滤食浮游植物,还摄食细菌,因此方形网纹溞可以同时从浮游植物和细菌处获得磷,从而比蚤状溞更有竞争优势[32].本研究中,在盔型溞和脆弱象鼻溞的混合培养中,碳磷比为105和740的处理组盔型溞种群密度分别为脆弱象鼻溞的55 %和75 %,而碳磷比为2400的处理组,两个种类的最大种群密度并没有差异.由于盔型溞平均体长超过1.5 mm,而脆弱象鼻溞的最大体长也不超过0.4 mm,因此,从生物量角度来看,在食物碳浓度超过它们的种群生长阈浓度时,盔型溞比脆弱象鼻溞更具有竞争优势,与“大小效率假说”预测的相符.盔型溞的种群增长率主要受磷限制,脆弱象鼻溞的存在对它没有影响.此外,在高度磷限制(食物碳磷比2400)时,脆弱象鼻溞能显著地降低盔型溞的最大种群密度,但在磷不限制或适度限制情况下,盔型溞的最大种群密度不受脆弱象鼻溞的影响.相反,不管食物是否磷缺乏,盔型溞的存在均能显著地影响脆弱象鼻溞的生长,降低脆弱象鼻溞的种群增长率和最大种群密度,而食物磷的缺乏进一步加大盔型溞对脆弱象鼻溞的影响程度. Urabe等[15]发现在食物磷限制条件下,溞可以通过提高磷的同化效率和增加摄食率来降低食物磷限制对个体生长率的影响.在食物磷限制条件下, 虽然盔型溞的个体变小,但仍然远远大于脆弱象鼻溞.因此,盔型溞的摄食率仍然高于脆弱象鼻溞.面对食物的磷限制,盔型溞可能通过增加摄食率和提高磷的同化效率来降低磷限制对其生长的影响程度,从而维持对脆弱象鼻溞的竞争优势.
在中国南亚热带地区水体中,广泛放养着滤食鱼类,盔型溞仅在鱼类捕食强度相对较低的季节(枯水期末期和丰水期早期)出现在水层中[21].虽然中国南亚热带地区水体属磷限制水体,枝角类的生长受磷限制,基于本研究的结果,盔型溞应该可以在与脆弱象鼻溞等小型枝角类的食物竞争中取得优势.但是,根据Lin等的研究结果看,盔型溞虽然在低鱼类捕食压力季节可以与小型枝角类同时出现在水体中,但其种群密度远低于小型枝角类种类,不是优势种类[21].综合以上的结果,我们认为虽然盔型溞对小型枝角类有竞争优势,而且这种优势基本上不受食物磷缺乏的影响,但鱼类的捕食使它们的竞争优势难以得到发挥.盔型溞在中国南亚热带地区水体中难以成为优势种的主要原因是浮游生物食性鱼类的捕食,而与食物的磷缺乏关系不大.尽管浮游生物食性鱼类的捕食压力有季节性变化,但在低捕食压力季节,浮游生物食性鱼类的捕食强度仍然足以阻止盔型溞成为优势浮游动物种类.
| [1] |
Mazumder A. Phosphorus-chlorophyll relationships under contrasting zooplankton community structure:potential mechanisms. Canadian Journal of Fisheries and Aquatic Sciences, 1994, 51: 401-407. DOI:10.1139/f94-041 |
| [2] |
Brooks JL, Dodson SI. Predation, body size, and composition of plankton. Science, 1965, 150: 28-35. DOI:10.1126/science.150.3692.28 |
| [3] |
Sarma SSS, Nandini S, Gulati RD. Life history strategies of cladocerans:comparisons of tropical and temperate taxa. Hydrobiologia, 2005, 542: 315-333. DOI:10.1007/s10750-004-3247-2 |
| [4] |
DeMott WR, Kerfoot WC. Competition among cladocerans:nature of the interaction between Bosmina and Daphnia. Ecology, 1982, 63(6): 1949-1966. DOI:10.2307/1940132 |
| [5] |
Jeppesen E, Meerhoff M, Holmgren K et al. Impacts of climate warming on lake fish community structure and potential effects on ecosystem function. Hydrobiologia, 2010, 646: 73-90. DOI:10.1007/s10750-010-0171-5 |
| [6] |
Lin Q, Xu L, Hou J et al. Response of trophic structure and zooplankton community to salinity and temperature in Tibetan lakes:Implication for the effect of climate warming. Water Research, 2017, 124: 618-629. DOI:10.1016/j.watres.2017.07.078 |
| [7] |
Ventura M. Linking biochemical and elemental composition in freshwater and marine crustacean zooplankton. Marine Ecology Progress Series, 2006, 327: 233-246. DOI:10.3354/meps327233 |
| [8] |
Elser JJ, Sterner RW, Gorokhova E et al. Biological stoichiometry from genes to ecosystems. Ecology Letters, 2000, 3: 540-550. DOI:10.1046/j.1461-0248.2000.00185.x |
| [9] |
Main TM, Dobberfuhl DR, Elser JJ. N:P stoichiometry and ontogeny of crustacean zooplankton:A test of the growth rate hypothesis. Limnology and Oceanography, 1997, 42(6): 1474-1478. DOI:10.4319/lo.1997.42.6.1474 |
| [10] |
Zhang Z, Ming R, Peng L et al. Nitrogen and phosphorus contents and excretion rate of seven common zooplankton in South China. J Lake Sci, 2017, 29(6): 1455-1463. [张振华, 明瑞梁, 彭亮等. 南亚热带水体7种常见浮游动物的个体氮、磷含量及其排泄率的比较. 湖泊科学, 2017, 29(6): 1455-1463. DOI:10.18307/2017.0617] |
| [11] |
Urabe J, Clasen J, Sterner RW. Phosphorus limitation of Daphnia growth:Is it real?. Limnology and Oceanography, 1997, 42(6): 1436-1443. DOI:10.4319/lo.1997.42.6.1436 |
| [12] |
Acharya K, Kyle M, Elser JJ. Biological stoichiometry of Daphnia growth:An ecophysiological test of the growth rate hypothesis. Limnology and Oceanography, 2004, 49(3): 656-665. DOI:10.4319/lo.2004.49.3.0656 |
| [13] |
Zhang H, Cai M, Chen FZ. Effects of Scenedesmus obliquus with different C/P ratios on the growth and reproduction of Daphnia similis. J Lake Sci, 2017, 29(5): 1188-1194. [张慧, 蔡敏, 陈非洲. 不同碳磷比的斜生栅藻(Scenedesmus obliquus)对同型溞(Daphnia similis)生长和繁殖的影响. 湖泊科学, 2017, 29(5): 1188-1194. DOI:10.18307/2017.0516] |
| [14] |
Elser JJ, Kyle M, Learned J et al. Life on the stoichiometric knife-edge:effects of high and low food C:P ratio on growth, feeding, and respiration in three Daphnia species. Inland Waters, 2016, 6: 136-146. DOI:10.5268/IW |
| [15] |
Urabe J, Shimizu Y, Yamaguchi T. Understanding the stoichiometric limitation of herbivore growth:the importance of feeding and assimilation flexibilities. Ecology Letters, 2018, 21: 197-206. DOI:10.1111/ele.12882 |
| [16] |
Branco P, Egas M, Elser JJ et al. Eco-evolution dynamics of ecological stoichiometry in plankton communities. The American Naturalist, 2018, 192(1): E000. DOI:10.1086/697472 |
| [17] |
Zhou L, Lemmen KD, Zhang W et al. Direct and indirect effects of resource P-limitation differentially impact population growth, life history and body elemental composition of a zooplankton consumer. Frontiers in Microbiology, 2018, 9: 172. DOI:10.3389/fmicb.2018.00172 |
| [18] |
Van Donk E, Hessen DO. Reduced digestibility of UV-B stressed and nutrient-limited algae by Daphnia magna. Hydrobiologia, 1995, 307: 147-151. DOI:10.1007/BF00032006 |
| [19] |
Van Donk E, Lürling M, Hessen DO et al. Changed cell wall morphology in nutrient deficient phytoplankton and its impact on grazers. Limnology and Oceanography, 1997, 42: 357-364. DOI:10.4319/lo.1997.42.2.0357 |
| [20] |
Challagulla V, Fabbro L, Nayar S. Biomass, lipid productivity and fatty acid composition of fresh water microalgal Rhopalosolen saccatus cultivated under phosphorus limited conditions. Algal Research, 2015, 8: 69-75. DOI:10.1016/j.algal.2015.01.010 |
| [21] |
Lin Q, Jiang X, Han BP et al. Does stocking of filter-feeding fish for production have a cascading effect on zooplankton and ecological state? A study of fourteen (sub)tropical Chinese reservoirs with contrasting nutrient concentrations. Hydrobiologia, 2014, 736: 115-125. DOI:10.1007/s10750-014-1896-3 |
| [22] |
Sommer U, Adrian R, De Senerpont Domis L et al. Beyond the plankton ecology group (PEG) model:mechanisms driving plankton succession. Annual Review of Ecology, Evolution, and Systematics, 2012, 43: 429-448. DOI:10.1146/annurev-ecolsys-110411-160251 |
| [23] |
Sibly RM, Hone J. Population growth rate and its determinants:an overview. Philos T Roy Soc B, 2002, 357: 1153-1170. DOI:10.1098/rstb.2002.1117 |
| [24] |
Lynch M. The evolution ofcladoceran life histories. The Quarterly Review of Biology, 1980, 55(1): 23-42. DOI:10.1086/411614 |
| [25] |
Elser JJ, Dobberfuhl DR, MacKay NA et al. Organism size, life history, and N:P stoichiometry. BioScience, 1996, 46(9): 674-684. DOI:10.2307/1312897 |
| [26] |
Vanni MJ. Competition in zooplankton communities:Suppression of small species by Daphnia pulex. Limnology and Oceanography, 1986, 31(5): 1039-1056. DOI:10.4319/lo.1986.31.5.1039 |
| [27] |
Schulz KL, Sterner RW. Phytoplankton phosphorus limitation and food quality for Bosmina. Limnology and Oceanography, 1999, 44(6): 1549-1556. DOI:10.4319/lo.1999.44.6.1549 |
| [28] |
Acharya K, Bukaveckas PA, Jack JD et al. Consumer growth linked to diet and RNA-P stoichiometry:Response of Bosmina to variation in riverine food resource. Limnology and Oceanography, 2006, 51(4): 1859-1869. DOI:10.4319/lo.2006.51.4.1859 |
| [29] |
Gulati RD, DeMott WR. The role of food quality for zooplankton:Remarks on the state-of-the-art, perspectives and priorities. Freshwater Biology, 1997, 38: 753-768. DOI:10.1046/j.1365-2427.1997.00275.x |
| [30] |
Iwabuchi T, Urabe J. Competitive outcomes between herbivorous consumers can be predicted from their stoichiometric demands. Ecosphere, 2012, 3(1): 7. |
| [31] |
DeMott WR, Van Donk E. Strong interactions between stoichiometric constraints and algal defenses:Evidence from population dynamics of Daphnia and algae in phosphorus-limited microcosms. Oecologia, 2013, 171: 175-186. DOI:10.1007/s00442-012-2404-y |
| [32] |
Iwabuchi T, Urabe J. Phosphorus acquisition and competitive abilities of two herbivorous zooplankton, Daphnia pulex and Ceriodaphnia quadrangula. Ecological Research, 2010, 25: 619-627. DOI:10.1007/s11284-010-0692-4 |
 2019, Vol. 31
2019, Vol. 31 

