(2: 南京师范大学环境学院, 南京 210023)
(2: School of Environment, Nanjing Normal University, Nanjing 210023, P. R. China)
河流是陆地系统主要的氮汇,每年向海洋输送的氮量约为35 Tg。氮素是我国河流的主要污染物之一,削减氮负荷是河流水环境管理和修复的关键问题。反硝化作用可使氮素以氮气(N2)形式彻底脱离水体,全球输入河流的总氮约有50 % 通过反硝化作用被去除[1-2],尽管已发现厌氧氨氧化、甲烷厌氧氧化等脱氮过程在河流中存在,但目前认为反硝化过程仍是河流氮去除的重要途径[3-4],是调节区域甚至全球尺度上氮循环的关键过程[1]。目前对河流反硝化作用的研究场所主要集中在沉积物-水界面和上覆水中,普遍认为河流沉积物由于含有丰富的有机质、氮(N)、磷(P)、硫(S)和微生物等,是反硝化发生的主要场所[2, 5]。
自然水环境中反硝化作用通常出现在很薄(μm~mm)的基质层内[6]。氮负荷较高的水体中,沉水植物茎叶表面常有一层附着生物膜,其结构和物质组成复杂,存在氧化-还原异质微环境[7-8],且营养物质丰富,是氮素循环及生命活动较为强烈的场所[9]。已发现在夏季养分和水生植物丰富的浅水河流和人工湿地中,沉水植物马来眼子菜(Potamogeton malainus Miq)、金鱼藻(Ceratophyllum demersum L.)、穗状狐尾藻(Myriophyllum spicatum L.)、苦草(Vallisneria natans),挺水植物芦苇(Phragmites australis)附着生物膜的反硝化活性较高,反硝化作用贡献(38.96 % ~67.56 %)已接近甚至超过沉积物的贡献[9-11],是不可忽视的反硝化场所。在富营养化水体中,沉水植物菹草(Potamogeton crispus)春季适宜温度(10~20℃)下暴发生长(“疯长”)可造成生物量(2.0~5.3 kg/m2)和盖度(>80 %)过大[12],可能会强烈影响水生态系统中的硝化、反硝化过程,促进氮去除。但相关研究非常匮乏,限制了河流氮收支的精确计算及氮汇的评价。
沂河是发源于山东省境内最长的河流,由于临沂市城区段受污水排放、橡胶坝及人类活动影响,水污染负荷压力较大,水体氮磷养分丰富,菹草已成为春季该水域的绝对优势种,每年4、5月份均有暴发现象,由菹草引发的水质污染问题成为已成为关注的焦点,常采用收割打捞的方式清除菹草,但对河流生态系统的干扰较大,且忽略了菹草的生态功能。暴发生长期菹草生物量增长迅速,为附着生物膜提供了巨大的附着表面,附着生物膜反硝化作用如何变化?单位河流面积上附着生物膜反硝化脱氮潜力有多大?其对水生态系统氮去除的贡献如何?是否河流反硝化作用的热点?这些问题目前尚不清楚,难以客观科学地评价菹草暴发生长对水体的环境效应。鉴于此,本研究选择沂河城区段菹草进行观测研究,主要目的是分析暴发生长阶段菹草附着生物膜的反硝化作用变化特征,探明附着生物膜反硝化脱氮潜力,为菹草的科学管控和生态系统服务功能的提高提供科学依据。
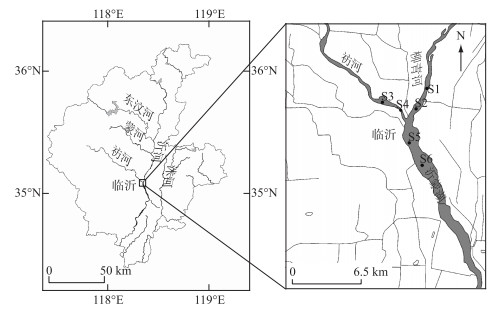
1 材料与方法 1.1 研究区概况在沂河临沂市城区段,沂河桃园橡胶坝与小埠东橡胶坝、角沂橡胶坝、刘家道口枢纽相连形成面积36 km2的沂蒙湖。经过近几年的生长繁殖,菹草已成为临沂市中心城区水域的绝对优势种,占所有沉水植物的90 % 以上,每年4月至5月中下旬,菹草覆盖大部分水面,生物量达到最大,阻挡了80 % 以上的光,抑制了水中浮游藻类的生长。白天菹草的光合作用较高,夜间由于菹草的呼吸作用可将水体中氧气(O2)消耗至1 mg/L以下[8],有利于反硝化作用进行。在前期野外调查基础上,选择沂河城区段6个典型样点(图 1)进行研究,各采样点水体理化特征、菹草丰富度存在差异(表 1),S1、S2样点菹草丰富度为中,S3、S4样点菹草丰富度高(图 2),S5、S6样点菹草丰富度低。在菹草快速生长季节(3月底至5月下旬)监测其丰富度变化。2019年从4月初开始在上述地点采集菹草、水和沉积物样品,至5月下旬菹草叶片出现大量分解时采样结束,每7~10天采样1次。
|
图 1 菹草观测点示意图 Fig.1 Sampling sites of Potamogeton crispus |
| 表 1 菹草暴发生长前采样点水体理化特征* Tab. 1 Parameters of river water at the sampling sites |

|
图 2 沂河采样点S3菹草暴发情况(2019年4月30日) Fig.2 Photographs of Potamogeton crispus during explosive growing at S3 in Yi River |
在每个采样点随机选择3个样方(0.5 m×0.4 m),样方间隔50~100 m,用水草夹小心采集每个样方的全部菹草装入无菌袋,然后在每个样方内用柱状采泥器采集完整沉积物底泥柱(深10 cm,直径8.4 cm)3个,采集表层水样2000 mL。用便携式参数检测仪(Hach, USA)在每样方现场测定水温(WT)、溶解氧(DO)、pH和氧化还原电位(Eh)等。取表层(0~5 cm)沉积物柱样,两端封好。植物、底泥和水样置于恒温保温箱中立即运回实验室。
本研究中菹草重量均为湿重。菹草全部称重后换算为生物量,取3~5株完整新鲜菹草用于反硝化培养实验,取10 g左右用于定量分析附着反硝化细菌;沉积物用于反硝化培养实验;水样用于分析硝态氮(NO3--N)、亚硝态氮(NO2--N)、氨氮(NH3-N)、总氮(TN)、总磷(TP)等指标。
1.3 反硝化作用样品的培养实验和产物N2的分析沉水植物附着生物膜反硝化采用连续流动培养法[13]。在接近原位条件下培养与测定。将菹草30 g左右移入培养系统中避光(模拟夜间黑暗条件)预培养24 h,使系统内O2消耗尽。将培养液(表 2)稀释100倍,加入15N同位素(Na15NO3),使培养液中15NO3-浓度为100 μmol/L,以加入未标记的NaNO3为对照,流速为1.0~1.4 mL/min,在原位温度下避光反应,培养时间3 d,分别在0、24、48、72 h后从取样口吸取溶液至气密型玻璃管中(3个平行样)。取样后立即往每个样品中加入0.2 mL浓度为50 % 的ZnCl2溶液终止微生物活性。沉积物柱亦采用连续流动培养方法测定反硝化和厌氧氨氧化速率,培养装置根据自有专利[13]和赵锋等[14]的装置进行改进。产生的N2用膜进样质谱仪(MIMS)测定,通过产生的N2浓度的变化计算相应的速率(3次的平均值)。其余水样中加入2 mL ZnCl2溶液终止微生物活性后用于NO3--N、NO2--N、NH3-N、TN和TP分析。菹草取出后用于后续附着生物分析。
| 表 2 实验中使用的营养液组成 Tab. 2 Constitution of the nutrient solution used in the experiments |
根据膜进样质谱仪测定的溶液中产生的28N2、29N2、30N2浓度,通过同位素配对计算反硝化作用速率和厌氧氨氧化作用速率[9, 15-16]。
| $ D_{\text {tot }}=P_{30} \cdot\left(F_{\mathrm{N}}^2\right) $ | (1) |
| $ A_{\text {total }}=F_{\mathrm{N}}^{-1} \times\left[P_{29}+2\left(1-F_{\mathrm{N}}^{-1}\right) \times P_{30}\right] $ | (2) |
式中,Dtot表示通过反硝化产生N2的量,Atotal表示通过厌氧氨氧化作用产生的N2量,FN表示NO3--N中15N的丰度(一般约为0.95),P29表示产生29N2的量,P30表示产生30N2的量。
为便于比较菹草附着生物膜反硝化作用、厌氧氨氧化作用和沉积物反硝化作用及厌氧氨氧化作用,将反硝化速率单位转换为通用单位μmol/(m2·h)。单位河流面积上菹草附着生物膜的反硝化作用速率和厌氧氨氧化速率通过菹草生物量(g/m2)、菹草样品占地面积(m2)、蠕动泵流速(mL/min)、N2的浓度(μmol/L)进行换算;单位河流面积上沉积物的反硝化速率和厌氧氨氧化速率根据沉积物柱横截面面积(m2)、蠕动泵流速(mL/min)、N2的浓度(μmol/L)进行换算。
1.5 附着生物膜样品的采集与分析反硝化作用实验结束后,取出菹草,洗脱附着生物膜[9]。附着生物膜干重(dry weight, DW)、TN、总有机碳(TOC)测定分析方法详见文献[9]。附着物TN、TOC采用总有机碳/总氮分析仪(multi N/C 3100,德国)测定。菹草叶面积采用LI-3000C便携式叶面积仪测定。水体TP、TN、NH3-N、NO3--N采用标准方法分析[17]。
附着反硝化细菌的定量分析采用荧光定量qPCR方法。用超声法洗脱附着细菌[9],真空抽滤至滤膜-80℃保存。附着细菌反硝化功能基因扩增与荧光定量分析委托上海美吉生物科技有限公司进行。DNA浓度和纯度使用Nanodrop 2000微量紫外分光光度计检测。反硝化功能基因nirK、nirS和 nosZ扩增使用引物及序列见表 3。使用ABI7500型荧光定量PCR仪进行扩增,扩增体系如下:2×ChamQ SYBR Color qPCR Master Mix 16.5 μL,上下游引物各0.8 μL,DNA模板2 μL,加无菌ddH2O水补足20 μL。所有样品进行3次重复扩增,最后所得功能基因拷贝数为3次重复的均值。扩增结果使用StepOne Software vv2.2.2进行人工校准。
| 表 3 定量扩增使用引物及反应程序 Tab. 3 Primer pairs and sequence used in qPCR |
利用SPSS 25.0软件对数据进行统计分析,利用单因素方差分析(ANOVA)分析不同日期附着生物膜反硝化速率的差异显著性,采用OriginPro 9.0软件绘图。
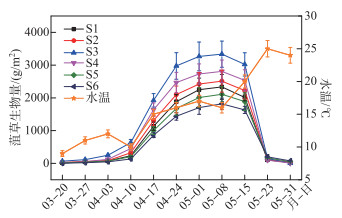
2 结果与分析 2.1 菹草暴发生长特征春季沂河临沂城区段菹草生长呈单峰变化模式(图 3),暴发生长阶段,菹草生物量呈指数增长趋势。3月下旬,6个监测点均有菹草零星出现,生物量(鲜重)为20~114 g/m2;随着水温升高,菹草生长加速,4月上旬,河岸浅水区菹草接近水面,分布面积明显增加,仍呈点状分布;4月中旬,菹草进入暴发生长阶段,生物量增长迅速(860~1926 g/m2),菹草沿河呈带状分布,宽度为30~50 m,随水温升高菹草扩展速度加快,菹草带明显增大。5月1日前后,在S3~S4河段,菹草布满河面,盖度在80 % 以上(图 2),菹草生物量、盖度持续增加,菹草进入繁殖期,结实大量芽殖体,菹草生长进入稳定阶段。5月8日,6个采样点生物量均达到最大(1817~3334 g/m2),在水面附近形成致密的冠层,分别为3月27日生物量的58.37、44.82、29.25、54.04、56.97、90.85倍。
|
图 3 菹草暴发性生长阶段生物量变化 Fig.3 Curves of Potamogeton crispus biomass during burst explosive growing stage |
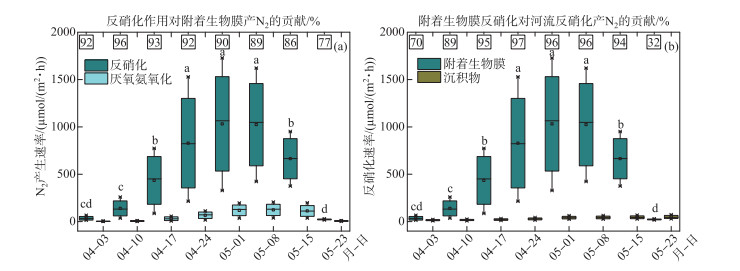
菹草暴发生长阶段,各采样点菹草附着生物膜反硝化速率迅速升高(图 4),与菹草生物量变化趋势一致。4月3日,各采样点菹草附着生物膜的反硝化速率均处于最低水平(2.12~8.38 μmol/(m2·h))。随着菹草生物量的增加和水温的升高,菹草附着生物膜反硝化速率显著升高,且明显高于沉积物的。暴发生长阶段,不同日期菹草附着生物膜反硝化作用差异显著,5月1日-5月8日,各采样点菹草附着生物膜的反硝化速率达到最大,分别为936.97、1192.82、1728.39、1337.33、686.71、424.18 μmol/(m2·h)。暴发生长期间,菹草附着生物膜反硝化脱氮远超过厌氧氨氧化,占比达77 % ~96 %。与菹草生物膜反硝化相比,沉积物的反硝化速率相对较低,且变化幅度较小(15.10~49.24 μmol/(m2·h))(图 4b)。
|
图 4 暴发生长期间菹草附着生物膜反硝化、厌氧氨氧化和沉积物反硝化速率 (箱图的上方和下方的线段分别表示第三四分位数和第一四分位数,箱图中间的线段表示中位数,箱图外最上方和最下方的线段表示范围从第5百分位到第95百分位) Fig.4 4 Rates of denitrification and anammox in epiphytic biofilms on Potamogeton crispus and rates of denitrification in sediments (Each box indicates the 25th and 75th percentiles, and horizontal line indicates median value, and whisker shows range from the 5th to 95th percentile) |
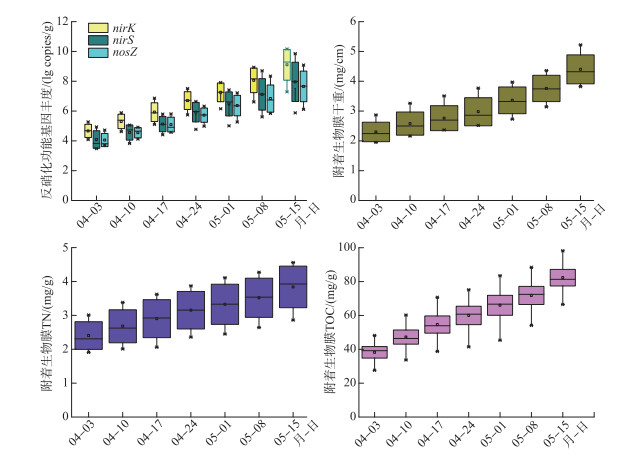
暴发生长阶段,随着菹草的快速生长,附着物干重逐渐增加,总细菌丰度、反硝化细菌功能基因nirK、nirS和 nosZ丰度以及TN、TOC含量均显著增加(图 5)。菹草附着物TOC含量(16.33~98.21 mg/g)和TN含量(1.65~4.56 mg/g)较高,附着物的养分量丰富,可为附着生物进行反硝化作用提供丰富的碳源和氮源。
|
图 5 菹草暴发生长期间附着生物膜各指标变化特征 Fig.5 Variation characteristics of epiphytic biofilms on Potamogeton crispus during explosive growing stage |
菹草暴发生长期间,在有污水持续排入、橡胶坝落坝未放水的情况下,沂河水体氮负荷仍有降低趋势(图 6)。水体中TN、NO3--N、NH3-N、NO2--N在5月8日前后降至最低值,水体透明度增加,之后随菹草的衰亡有所升高。

|
图 6 菹草暴发生长期间水体氮浓度变化 Fig.6 Variation characteristics of nitrogen concentration in water during Potamogeton crispus explosive growing stage |
本研究发现,菹草暴发生长阶段,菹草生物量快速增加,菹草叶片表面积激增,叶片表面的附着生物膜可吸附大量的NO3--N和颗粒氮,可为反硝化作用提供底物,是大幅度促进附着生物膜反硝化作用的关键。富营养化沂河城区段菹草暴发性生长除大量吸收水体中的NO3--N外,较大的覆盖度、夜间造成的附着生物膜微氧和水下缺氧环境为反硝化作用的发生提供了有利条件,提高了通过反硝化作用去除水体氮素的能力。菹草暴发生长会强烈影响水生态系统中的硝化-反硝化过程。白天,密集的菹草种群强烈光合作用使水体和附着生物膜产生富氧环境,附着生物膜O2浓度可达521~800 μmol/L[8],利于硝化作用进行,夜间,密集菹草通过呼吸作用和微生物活动显著降低水体和附着生物膜中O2浓度,易使水体和附着生物膜产生低氧甚至缺氧条件[9, 23-24],有利于反硝化作用的发生。菹草暴发生长期间,O2浓度的昼夜变化可能会导致水体白天发生硝化作用、夜间发生反硝化作用的现象。由于菹草附着生物膜环境异质性较大,易形成好氧-缺氧微生境,硝化作用和反硝化作用则可能同时发生。
春末夏初,在菹草暴发生长阶段(4月中旬-5月中旬),沂河、祊河城区段菹草生物量可达1817~3334 g/m2,覆盖面积可达30 % ~90 %。当按菹草单位叶表面积来计算附着生物膜的反硝化速率时,它远低于沉积物的反硝化速率,但当按单位河流面积计算时,附着生物膜的反硝化速率则高于沉积物的。以5月1日各采样点为例,菹草附着生物膜的反硝化速率高达424.18~1728.39 μmol/(m2·h),而沉积物反硝化速率为24.53~62.45 μmol/(m2·h),是表层沉积物反硝化速率的17.29~29.09倍,占该日通过反硝化作用氮去除总量的96 %,成为反硝化作用的热点区域。在菹草暴发期间,菹草生物膜通过反硝化作用产生的N2可占河流反硝化脱氮作用的70 % ~97 % (图 4b)。类似的高反硝化速率在其他富营养化水体亦有发现,蓝藻水华期太湖水柱的反硝化速率可达(534.45±242.18)~(1614.52±301.57) μmol/(m2·h)[25],Hudson河岸带入侵植物菱Trapa natans丰富的区域反硝化速率高达1541.7~2958.3 μmol/(m2·h)[10]。
本研究发现,在有外源氮持续输入的情况下,菹草暴发阶段沂河水体的TN浓度并未升高,可能菹草在沂河氮去除过程中发挥着重要作用。通常,NO3--N同化还原为NH4+(DNRA)是沉积物中NO3--N转化的一个重要途径,但沂河河床底部多为岩石,沉积物层较薄,该过程在沂河沉积物中比较弱,沉积物的氮去除能力有限;菹草暴发期间,水体中Chl.a浓度较低,浮游藻类对氮的吸收量也相对较少。尹传宝等[26]通过控制实验发现,在无外源氮输入的情况下菹草对氮负荷的降低非常显著,菹草对TN的吸收率为50.66 % ~67.81 %,对NH3-N的吸收率为86.44 %,对NO3--N的吸收率为12.26 % ~36.75 %;水体中NO3--N浓度与反硝化功能基因丰度呈正相关,NO3--N浓度增加可刺激附着反硝化细菌增殖[27-28]。本研究结果表明沂河菹草附着生物膜的厌氧氨氧化作用贡献也相对较小(图 3),据此可以推测,菹草对氮的吸收和附着生物膜反硝化可能是沂河临沂城区段水体氮去除的主要途径,附着生物膜反硝化是氮素以气体形式损失的主要途径。沉水植物菹草虽然只有春季3~4个月的活跃期,1个月左右的暴发生长期,但它们为附着生物膜提供了巨大的附着面积,附着生物膜的反硝化作用贡献较大,是城市河流沂河祊河生态系统氮去除的重要环节,无论是进行河流生态管理,还是进行氮循环预算,应引起足够重视,不可忽略。菹草生命周期与多数水生植物不同,在秋季发芽,冬季由于中国北方水温较低在水下生长缓慢,观测和采样难度较大,所以本研究仅对春季和夏初的菹草附着生物膜反硝化进行了研究,可能不能精确地评估生物膜反硝化作用对河流反硝化作用的总贡献。今后的研究中,将原位观测与控制实验结合,分析菹草生物膜反硝化作用的季节动态,可解决这一问题,也可对菹草的科学管理提供更全面的科学依据。
3.2 菹草的科学管理建议研究表明,当菹草生物量超过2000 g/m2即可视为过度生长(暴发)[12],依据这一标准,本研究6个监测点中有5个点达到了暴发水平。目前相关管理部门普遍认为彻底清除菹草是解决菹草引发的水质污染问题的有效方法。本研究认为,通过科学管理,充分利用菹草强大的养分吸收功能和附着生物膜高效的反硝化脱氮功能降低水污染负荷更有助于解决问题,提高河流生态系统的服务功能。建议如下:
1) 构建镶嵌型水生植物群落。可在沂河菹草区种植本地物种金鱼藻、穗状狐尾藻、黑藻(Hydrilla verticillata Royle)等沉水植物,春末生根发芽,夏初菹草衰亡时长至水面,使沉水植物群落有效交替,充分发挥沉水植物附着生物膜的生态功能,可缓解菹草衰亡带来的不利影响。
2) 适度收割。合理地收割既有利于沉水植物的恢复和生长,又可缓解生物量过度集中于水体表层的趋势,提高群落持续净化水质的稳定性。在菹草生长中期对其进行60 % ~80 % 收割,可控制菹草过度生长,并维持水体养分负荷在较低水平[29]。因此,可以通过适时、适量收割来控制沂河城区段菹草暴发,理想割草时间为4月下旬,此时芽殖体尚未发育成熟,避免来年菹草大面积发生。使其既能充分发挥其生物脱氮作用,又可避免因密集衰亡分解对水环境造成的负面影响。
3) 调控水位。假设透明度保持不变,水位提高1 m,水下太阳辐照度将降低56.5 %,可显著降低菹草所需的光照,从而抑制菹草生长[30]。4月是沂河祊河菹草生长的关键时期,在条件允许的情况下,可以利用橡胶坝的调蓄功能适当增加河流蓄水量,抬高水位,进而抑制其过度生长。
4 结论1) 4月上旬-5月初为营养丰富的沂河菹草暴发增长期,生物量增加迅速,5月8日监测点最大生物量为1817~3334 g/m2。
2) 暴发生长阶段,菹草附着生物膜厚度和干重逐渐增加,反硝化功能基因丰度、TOC、TN均显著增加,为附着生物膜反硝化作用提供了丰富的能源和微环境条件。
3) 暴发生长期,菹草附着生物膜成为反硝化作用热点。菹草附着生物膜反硝化作用最大速率为424.18~ 1728.39 μmol/(m2·h),是表层沉积物反硝化作用的17.29~29.09倍。菹草附着生物膜反硝化作用是沂河临沂城区段春季生态系统氮去除的重要环节,环境意义重大。
4) 可通过构建镶嵌型沉水植物群落、适度收割、调控水位等措施来缓解菹草暴发,提高河流生态系统的服务功能。
| [1] |
Schlesinger WH, Reckhow KH, Bernhardt ES. Global change: The nitrogen cycle and rivers. Water Resources Research, 2006, 42(3): 1-2. DOI:10.1029/2005wr004300 |
| [2] |
Ma P, Li XY, Wang HX et al. Denitrification and its role in cycling and removal of nitrogen in river. Journal of Agro-Environment Science, 2014, 33(4): 623-633. [马培, 李新艳, 王华新等. 河流反硝化过程及其在河流氮循环与氮去除中的作用. 农业环境科学学报, 2014, 33(4): 623-633. DOI:10.11654/jaes.2014.04.002] |
| [3] |
Liu C, Hou LJ, Liu M et al. Coupling of denitrification and anaerobic ammonium oxidation with nitrification in sediments of the Yangtze Estuary: Importance and controlling factors. Estuarine, Coastal and Shelf Science, 2019, 220: 64-72. DOI:10.1016/j.ecss.2019.02.043 |
| [4] |
Groh TA, Isenhart TM, Schultz RC. Long-term nitrate removal in three riparian buffers: 21 years of data from the Bear Creek watershed in central Iowa, USA. The Science of the Total Environment, 2020, 740: 140114. DOI:10.1016/j.scitotenv.2020.140114 |
| [5] |
Chen ZY, Zhang TN, Zhang ZW et al. Aerobic denitrifying bacteria community structure and response of aerobic denitrifying bacteria to dissloved organic matter in the sediments in Lake Baiyangdian in the spring. J Lake Sci, 2022, 34(2): 538-552. [陈召莹, 张甜娜, 张紫薇等. 白洋淀春季沉积物好氧反硝化菌群落结构特征及对溶解性有机物的响应. 湖泊科学, 2022, 34(2): 538-552. DOI:10.18307/2022.0215] |
| [6] |
Revsbech NP, Risgaard-Petersen N, Schramm A et al. Nitrogen transformations in stratified aquatic microbial ecosystems. Antonie Van Leeuwenhoek, 2006, 90(4): 361-375. DOI:10.1007/s10482-006-9087-5 |
| [7] |
Li Q, Gu P, Ji XY et al. Response of submerged macrophytes and periphyton biofilm to water flow in eutrophic environment: Plant structural, physicochemical and microbial properties. Ecotoxicology and Environmental Safety, 2020, 189: 109990. DOI:10.1016/j.ecoenv.2019.109990 |
| [8] |
Dong B, Han RM, Wang GX et al. Mciro-optode analysis of the spatio-temporal dynamics of O2 in the micro-boundary layer around Potamogeton crispus leaves and stems. Acta Ecoloica Sinica, 2015, 35(24): 8202-8210. [董彬, 韩睿明, 王国祥等. 菹草茎叶微界面O2时空动态. 生态学报, 2015, 35(24): 8202-8210. DOI:10.5846/stxb201406101195] |
| [9] |
董彬, 王国祥, 马杰. 淡水附植生物的组成结构特征及其生态功能. 北京: 化学工业出版社, 2018.
|
| [10] |
Tall L, Caraco N, Maranger R. Denitrification hot spots: Dominant role of invasive macrophyte Trapa natans in removing nitrogen from a tidal river. Ecological Applications, 2011, 21(8): 3104-3114. DOI:10.1890/11-0061.1 |
| [11] |
Toet S, Huibers LHFA, Van Logtestijn RSP et al. Denitrification in the periphyton associated with plant shoots and in the sediment of a wetland system supplied with sewage treatment plant effluent. Hydrobiologia, 2003, 501(1/2/3): 29-44. DOI:10.1023/A:1026299017464 |
| [12] |
Zhang C, Chen XJ, Wang LY et al. Impact of excessive growth of Potamogeton crispus on water quality and cause analysis in Yuqiao Reservoir. Journal of Tianjin University, 2011, 44(1): 1-6. [张晨, 陈孝军, 王立义等. 于桥水库菹草过度生长对水质的影响及成因分析. 天津大学学报, 2011, 44(1): 1-6.] |
| [13] |
董彬, 王国祥, 于洪刚. 一种测定水生植物附着生物反硝化作用的培养装置: 中国, 201620767466.9.
|
| [14] |
Zhao F, Xu H, Zhan X et al. Spatial differences and influencing factors of denitrification and anammox rates in spring and summer in Lake Taihu. Environmental Science, 2021(5): 2296-2302. [赵锋, 许海, 詹旭等. 太湖春夏两季反硝化与厌氧氨氧化速率的空间差异及其影响因素. 环境科学, 2021(5): 2296-2302.] |
| [15] |
Nielsen LP. Denitrification in sediment determined from nitrogen isotope pairing. FEMS Microbiology Letters, 1992, 86(4): 357-362. DOI:10.1016/0378-1097(92)90800-4 |
| [16] |
Thamdrup B, Dalsgaard T. Production of N2 through anaerobic ammonium oxidation coupled to nitrate reduction in marine sediments. Applied and Environmental Microbiology, 2002, 68(3): 1312-1318. DOI:10.1128/AEM.68.3.1312-1318.2002 |
| [17] |
国家环境保护总局. 地表水环境质量标准(GB 3838—2002). 北京: 中国环境科学出版社, 2002.
|
| [18] |
Palmer K, Biasi C, Horn MA. Contrasting denitrifier communities relate to contrasting N2O emission patterns from acidic peat soils in Arctic tundra. The ISME Journal, 2012, 6(5): 1058-1077. DOI:10.1038/ismej.2011.172 |
| [19] |
Han XL, Huang CG, Zhang YX et al. NirS-type denitrifiers community composition and function in different riparian vegetation types in upper Wenyuhe watershed. Acta Ecoloica Sinica, 2020, 40(6): 1977-1989. [韩晓丽, 黄春国, 张芸香等. 文峪河上游河岸带不同植被类型土壤NirS反硝化菌群结构及功能. 生态学报, 2020, 40(6): 1977-1989. DOI:10.5846/stxb201906241331] |
| [20] |
Throbäck IN, Enwall K, Jarvis Å et al. Reassessing PCR primers targeting nirS, nirK and nosZ genes for community surveys of denitrifying bacteria with DGGE. FEMS Microbiology Ecology, 2004, 49(3): 401-417. DOI:10.1016/j.femsec.2004.04.011 |
| [21] |
Petersen DG, Blazewicz SJ, Firestone M et al. Abundance of microbial genes associated with nitrogen cycling as indices of biogeochemical process rates across a vegetation gradient in Alaska. Environmental Microbiology, 2012, 14(4): 993-1008. DOI:10.1111/j.1462-2920.2011.02679.x |
| [22] |
Kloos K, Mergel A, Rösch C et al. Denitrification within the genus azospirillum and other associative bacteria. Australian Journal of Plant Physiology, 2001, 28(9): 991-998. |
| [23] |
Sand-Jensen K, Revsbech NP, Jørgensen BB. Microprofiles of oxygen in epiphyte communities on submerged macrophytes. Marine Biology, 1985, 89(1): 55-62. DOI:10.1007/BF00392877 |
| [24] |
Wang JQ, Zheng YF, Wang GX. Iinfluences of Potamogeton Crispus population on the lake water quality distribution. Environmental Science, 2011, 32(2): 416-422. [王锦旗, 郑有飞, 王国祥. 菹草种群对湖泊水质空间分布的影响. 环境科学, 2011, 32(2): 416-422.] |
| [25] |
Liu ZY, Xu H, Zhan X et al. Influence of cyanobacterial blooms on denitrification rate in shallow Lake Taihu, China. Environmental Science, 2019, 40(3): 1261-1269. [刘志迎, 许海, 詹旭等. 蓝藻水华对太湖水柱反硝化作用的影响. 环境科学, 2019, 40(3): 1261-1269. DOI:10.13227/j.hjkx.201808056] |
| [26] |
Yin CB, Wang L, Zhang CY et al. Effect of Potamogeton crispus on different species of nitrogen in spring. China Rural Water and Hydropower, 2014(3): 9-11, 15. [尹传宝, 王龙, 张翠英等. 春季菹草对水体中各形态氮的作用效果研究. 中国农村水利水电, 2014(3): 9-11, 15.] |
| [27] |
Zhang ZQ, Chen HZ, Mu XY et al. Nitrate application decreased microbial biodiversity but stimulated denitrifiers in epiphytic biofilms on Ceratophyllum demersum. Journal of Environmental Management, 2020, 269: 110814. DOI:10.1016/j.jenvman.2020.110814 |
| [28] |
Yan LY, Zhang SH, Lin D et al. Nitrogen loading affects microbes, nitrifiers and denitrifiers attached to submerged macrophyte in constructed wetlands. Science of the Total Environment, 2018, 622/623: 121-126. DOI:10.1016/j.scitotenv.2017.11.234 |
| [29] |
Xu WW, Hu WP, Deng JC et al. Influence of harvesting Potamogeton crispus in a submerged plant community on the growth of submerged aquatic plants and their effects on water quality. Ecology and Environmental Sciences, 2015, 24(7): 1222-1227. [徐伟伟, 胡维平, 邓建才等. 菹草生物量控制对群落中沉水植物生长及水质的影响. 生态环境学报, 2015, 24(7): 1222-1227.] |
| [30] |
Dong BL, Zhou YQ, Jeppesen E et al. Response of community composition and biomass of submerged macrophytes to variation in underwater light, wind and trophic status in a large eutrophic shallow lake. Journal of Environmental Sciences, 2021, 103: 298-310. DOI:10.1016/j.jes.2020.11.027 |
 2023, Vol. 35
2023, Vol. 35 

